Imunokompromitirani bolesnik je u povećanoj opasnosti od infekcija kako uobičajenim, tako i oportunističkim uzročnicima.
INFEKCIJE U ONKOLOŠKIH BOLESNIKA
U Tbl. 79-1 navedene su normalne prepreke protiv infekcije čije oštećenje može omogućiti infekcije u imunokompromitiranih bolesnika, a posebice u onih s malignom bolešću. Mortalitet povezan s infekcijama među onkološkim bolesnicima se smanjuje kao rezultat ranog, empirijskog davanja antibiotika širokog spektra; empirijskog liječenja neutropeničnih bolesnika antifungicima koji nakon 4–7 dana antibiotskog liječenja ostaju febrilni bez pozitivnih bakterijskih kultura; te korištenja antibiotika kod afebrilnog neutropeničnog bolesnika u profilaksi infekcija.
TABLICA 79-1 PREKID NORMALNIH PREPREKA KOJI MOŽE POGODOVATI INFEKCIJAMA KOD ONKOLOŠKIH BOLESNIKA
|
|
Oblik obrane
|
Specifična lezija
|
Zahvaćene stanice
|
Uzročnik
|
Povezanost s karcinomom
|
Bolest
|
|
Fizička prepreka
|
Pukotine u koži
|
Stanice epitela kože
|
Stafilokoki, streptokoki
|
Glava i vrat, karcinom pločastih stanica
|
Celulitis, proširene kožne infekcije
|
|
Pražnjenje naku-pljenih tekućina
|
Začepljenje otvora: mokraćovoda, žučnih vodova, debelog crijeva
|
Epitelne stanice lumena
|
Gram-negativnibacili
|
Bubreg, jajnici, žučni vodovi, metastatsko širenje mnogih oblika raka
|
Brza, teška bakterijemija, infekcija mokra-ćnog sustava
|
|
Bolest limfnih putova
|
Disekcija čvora
|
Limfni čvorovi
|
Stafilokoki, streptokoki
|
Operacija raka dojke
|
Celulitis
|
|
Odstra-njenje mikroorganizama u slezeni
|
Splenektomija
|
Retikulo-endotelne staniceslezene
|
Streptococcus pneumoniae, Haemophilus influenzae, Neisseria meningitidis, Babesia, Capnocytophaga canimorsus
|
Hodgkinova bolest, leukemija
|
Brza, teška sepsa
|
|
Fagocitoza
|
Nedostatak granulocita
|
Granulociti (neutrofili)
|
Stafilokoki, streptokoki, crijevni mikroorganizmi, gljivice
|
Akutna mijelocitna i akutna limfocitna leukemija, leukemija vlasastih stanica
|
Bakterijemija
|
|
Humoralna imunost
|
Nedostatak protutijela
|
B-stanice
|
S. pneumoniae, H. influenzae, N. meningitidis
|
Kronična limfocitna leukemija, multipli mijelom
|
Infekcije očahurenim uzročnicima, sinusitis, pneumonija
|
|
Stanična imunost
|
Nedostatak T-stanica
|
T-stanice i makrofagi
|
Mycobacterium tuberculosis, Listeria, herpesvirusi, gljivice, intracelularni paraziti
|
Hodgkinova bolest, leukemija, T-stanični limfom
|
Infekcije intracelularnim bakterijama, gljivicama, parazitima; reaktivacija virusa
|
SINDROMI SPECIFIČNI ZA ORGANSKI SUSTAV
- Kožne infekcije: Lezije kože azličitih tipova česte su u bolesnika s karcinomom i mogu biti prvi znak bakterijske ili gljivične sepse, posebice u neutropeničnih bolesnika (odnosno s <500 funkcionalnih neutrofila/µl).
– Celulitis: najčešće uzrokovan streptokokima grupe A i Staphylococcus aureus. Neuobičajeni mikroorganizmi (Escherichia coli, Pseudomonas ili gljivica) također mogu biti uzročnik u neutropeničnih bolesnika.
– Makule ili papule: uzrokovane bakterijama (npr. s Pseudomonas aeruginosa koji uzrokuje ecthyma gangrenosum) ili gljivicama (Candida)
– Sweetov sindrom ili febrilna neutrofilna dermatoza: Najčešće se viđa u neutropeničnih bolesnika (posebice onih s akutnom mijeloidnom leukemijom); prezentira se kao crvene ili plavkasto-crvene papule ili čvorovi koji tvore oštro ograničene plakove; visokom temperaturom; ubrzanom sedimentacijom eritrocita. Ove su kožne lezije najčešće na licu, vratu i rukama.
– Erythema multiforme sa zahvaćanjem sluznica: Najčešće uzrokovan herpes simplex virusom (HSV), treba ga razlikovati od Stevens-Johnsonovog sindroma, koji je povezan s lijekovima i koji se češće javlja. Oba stanja česta su u bolesnika s karcinomom.
– Osip zbog lijekova: osip koji je povezan s lijekovima, posebice citokinima koji se koriste u liječenju karcinoma, komplicira diferencijalnu dijagnozu osipa u bolesnika s karcinomom.
- Infekcije u vezi s kateterom: Infekcije izlaznog mjesta, s eritemom oko insercijskog mjesta su najčešće.
– Infekcije uzrokovane koagulaza negativnim stafilokokima mogu se liječiti bez odstranjenja katetera.
– Infekcije uzrokovane drugim uzročnicima, uključujući Staphylococcus aureus, P. aeruginosa, Candida, Stenotrophomonas ili Bacillus, obično zahtijevaju odstranjenje katetera.
– If a red streak develops over the SC part of a “tunneled” catheter, the device must be removed to prevent extensive cellulitis and tissue necrosis.
- Infekcije gornjeg GI sustava: Oštećenja mukoznih površina su česta zbog kemoterapije i infekcija.
– Oralni mukozitis povezan s viridans streptokokima i HSV.
– Oralne kandida infekcije (soor) su česte.
– Ezofagitis može biti uzrokovan C. albicans i HSV.
- Infekcije donjeg GI sustava: Transmigracija crijevne flore preko crijevnog epitela može dovesti do ozbiljnih stanja.
– Kronična diseminirana kandidijaza: nastaje zasijavanjem organa (npr. jetre, slezene, bubrega) tijekom neutropenije u bolesnika s hematološkom zloćudnom bolešću, ali se očituje simptomima kad se neutropenija popravi. Bolesnici imaju stalnu vrućicu koja ne odgovara na antibiotike, bol u trbušnoj šupljini, mučninu i povišene razine alkalne fosfataze. Iako biopsija može otkriti granulome, kvasce ili pseudohife, dijagnoza se obično postavlja na temelju radioloških pretraga (CT, MR). Liječenje se usmjerava prema uzročniku; C. albicans obično dobro odgovara na terapiju, ali su često uključene C. tropicalis i ostale Candida vrste.
– Tiflitis (nekrotizirajući kolitis): češći u djece nego u odraslih te u bolesnika s akutnom mijelocitnom leukemijom ili akutnom limfocitnom leukemijom (ALL) nego u bolesnika s drugim oblicima raka. Bolesnici imaju vrućicu, bolnost u desnom donjem kvadrantu abdomena te proljev koji je često krvav. Dijagnoza se potvrđuje dokazivanjem zadebljanja stijenke cekuma radiološkim pretragama. Liječenje uključuje antibiotike koji djeluju na crijevnu floru te kirurški zahvat (u slučaju perforacije).
- Infekcije CNS-a: Osjetljivost bolesnika na specifičnu infekciju ovisi o tome da li imaju prolongiranu neutropeniju, oštećenje stanične imunosti (npr. zbog visokih doza glukokortikoida ili citotoksične kemoterapije) ili humoralne imunosti (npr. bolesnici s kroničnom limfocitnom leukemijom, prethodno splenektomirani ili s transplantiranom koštanom srži [BMT]).
– Meningitis: U obzir dolaze Cryptococcus ili Listeria, posebice u bolesnika s oštećenjem stanične imunosti. Splenektomirani bolesnici te oni s hipogamaglobulinemijom su također u opasnosti od infekcija inkapsuliranim bakterijama poput Streptococcus pneumoniae, Haemophilus influenzae i Neisseria meningitidis.
– Encefalitis: Bolesnici s oštećenjem stanične imunosti su posebice skloni infekcijama s VZV, JC virusom (uzročnikom progresivne multifokalne leukoencefalopatije), CMV, Listeria, HSV i humanim herpesvirusom tip 6.
– Mase u mozgu: najčešće se ispoljavaju kao glavobolja sa i bez vrućice ili neuroloških poremećaja. Bolesnici s prolongiranom neutropenijom imaju veći rizik za apscese mozga uzrokovane Aspergillus, Nocardia ili Cryptococcus. Bolesnici s oštećenjem stanične imunosti imaju veći rizik za infekciju s Toxoplasma gondii i EBV (limfoproliferativnu bolest). Definitivna dijagnoza može zahtijevati biopsiju.
- Plućne infekcije: Pneumonija se u imunokompromitiranih bolesnika ponekad teško dokazuje budući da se većina uobičajenih simptoma (npr. purulentni sputum, fizikalni nalazi sukladni plućnoj konsolidaciji) vezuje za prisustvo neutrofila. radiološki oblici infiltracije mogu pomoći sužavanju diferencijalne dijagnoze.
– Lokalizirani infiltrati: sumnjati na bakterijsku pneumoniju (uključujući Legionella i mikobakterije), lokaliziranu hemoragiju ili embolizaciju i tumor.
– Nodularni inflitrati: sumnjati na gljivičnu infekciju (Aspergillus, Mucor), Nocardia infekciju i rekurirajući tumor. U bolesnika s Aspergillus infekcijom, hemoptiza može biti upozoravajući simptom. Biopsija s izravnom vizualizacijom može biti nephodna za definitivnu dijagnozu.
– Difuzni infiltrati: U obzir dolaze virusi (posebice CMV), Chlamydia, Pneumocystis, Toxoplasma i mikobakterije. Virusi koji u normalnog domaćina uzrokuju infekcije gornjeg dišnog sustava (npr. virus gripe, respiratorni sincicijski virus) mogu uzrokovati smrtonosni pneumonitis u imunokompromitiranih. Neinfektivni uzroci uključuju radijacijski pneumonitis, kronično zatajenje srca, difuzno alveolarno krvarenje (nakon transplantacije koštane srži), te lijekovima izazvano oštećenje pluća (npr. bleomicin, alkilirajući agensi).
- Infekcije bubrega i uretera: Obično su povezane s opstruirajućim tumorskim masama.
– Candida pokazuje sklonost prema infekciji bubrega, do kojih dolazi ili hematogenim rasapom ili retrogradnim širenjem iz mjehura. Perzistirajuća fungurija mora upozoriti i na moguću infekciju bubrega (npr. “gljivičnu loptu”).
– BK i adenovirus mogu uzrokovati hemoragični cistitis.
PRISTUP BOLESNIKU:
Febrilna neutropenija
Pristup dijagnostici i liječenju febrilnih neutropeničnih bolesnika. Slika 79-1 predstavlja postupnik za dijagnostiku i liječenje bolesnika s febrilnom neutropenijom.
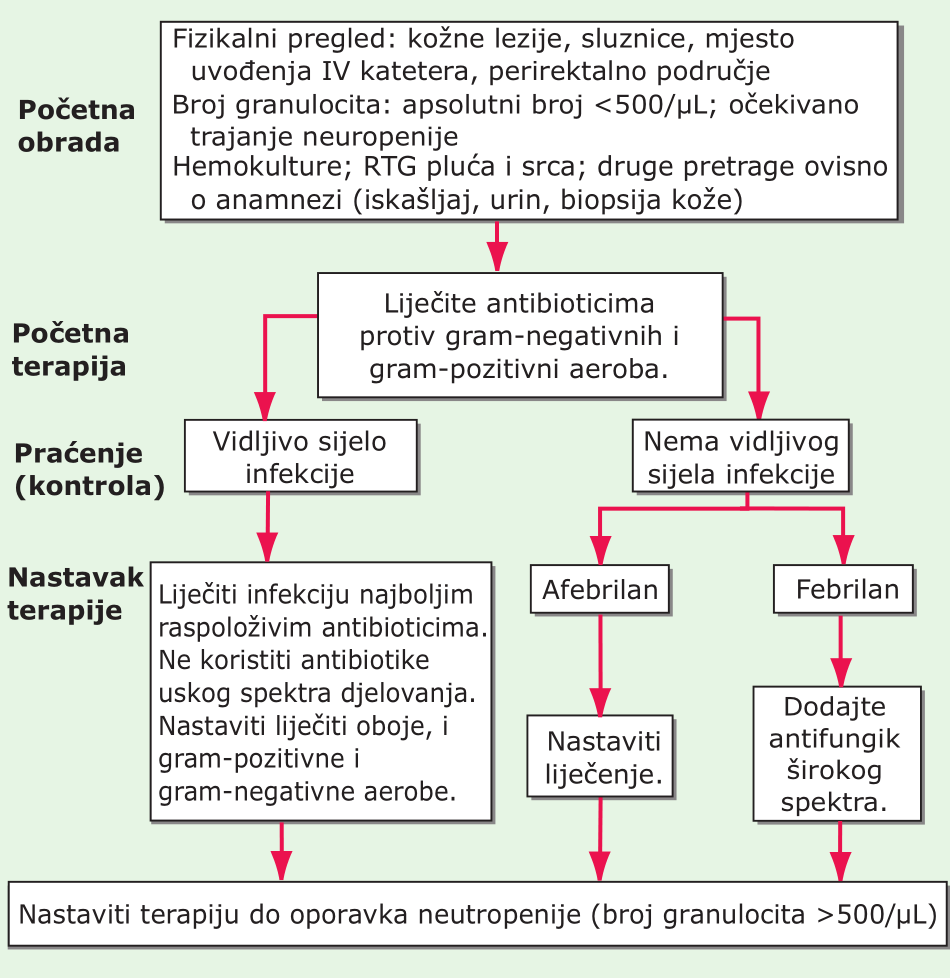
SLIKA 79-1 Postupnik za dijagnostiku i liječenje neutropeničnih bolesnika s vrućicom. Pri početnom liječenju tih bolesnika korisno je nekoliko općih naputaka: (1.) Lijekovi koji se koriste moraju odražavati kako epidemiologiju tako i raspodjelu otpornih izolata unutar bolnice. (2.) Cefalosporin treće generacije predstavlja dobru terapijsku opciju za inicijalno liječenje u većini bolnica (ako mu osjetljivost bakterija na antibiotike opravdava korištenje). (3.) Većina standardnih terapijskih opcija namijenjena je bolesnicima koji nisu profilaktički dobivali antibiotike. Pojava vrućice u bolesnika koji je dobio antibiotik utječe na izbor sljedećeg antibiotika (koji mora biti usmjeren i na otpornog mikroorganizma kao i mikroorganizma koji je uzrokovao infekciju koja je liječena s tim antibiotikom). (4.) Randomizirana istraživanja ukazala su kako nije opasno primijeniti oralno liječenje antibioticima pri liječenju “niskorizičnih” bolesnika s vrućicom i neutropenijom. Izvanbolnički bolesnici za koje se očekuje da će ostati neutropenični <10 dana i koji nemaju istovremenih zdravstvenih tegoba (kao što je hipotenzija, ugroženost pluća ili bol u trbušnoj šupljini), mogu se svrstati u niskorizične i liječiti peroralnim načinom, antibioticima širokog spektra.
- Početni terapijski režim se može mijenjati nakon rezultata kulture; površinski obrisci kože i sluznica mogu zavarati.
- Dodavanje antibiotika inicijalnoj terapiji nije opravdano ukoliko za to ne postoji klinički ili mikrobiološki razlog. Dodavanje antibiotika od straha zbog moguće infekcije gram-negativnim bakterijama (npr. “dvostruko pokrivanje”, odnosno dodavanje aminoglikozida β-laktamskim antibioticima) ne pojačava učinak (a može pojačati toksičnost) čak i u infekcijama uzrokovanim P. aeruginosa
- Za empirijsku antifungalnu terapiju, amfotericin B danas potiskuje liposomalna formulacija istog, noviji azoli (npr. vorikonazol ili posakonazol) te ehinokandini (npr. kaspofungin). Ehinokandini su korisni u infekcijama uzrokovanim na azole-otpornim kandidama.
- Klinička iskustva vezana za entivirusnu terapiju uglavnom su najbogatija za aciklovir u HSV i VZV infekcijama. Noviji lijekovi (npr. cidofovir, foskarnet) sa širim spektrom djelovanja usmjereli su pažnju na liječenje virusnih infekcija.
– Profilaktičko davanje antibiotika (npr. fluorokinolona) bolesnicima koji imaju prolongiranu neutropeniju ili protugljivičnih lijekova (npr. flukonazola) u bolesnika s presadcima hematopetskih matičnih stanica (vidi niže u tekstu) može spriječiti infekciju. Pneumocysitis profilaksa je obvezna u bolesnika s akutnom limfocitnom leukemijom i onima koji dobivaju glukokortikoide.
INFEKCIJE U TRANSPLANTIRANIH BOLESNIKA
Procjena infekcije u primalaca presadaka mora obuhvatiti u razmatranje uzročnika infekcije koji je u donoriranom organu kao i imunosupresivni terapijski režim primaoca, koji utječe na povećanu osjetljivost prema latentnim infekijama (među ostalima).
- Pretransplantacijska obrada davalaca mora uključivati potpunu serološku evaluaciju virusnih uzročnika (npr. HSV-1, HSV-2, VZV, CMV, EBV, HIV te hepatitis A, B i C viruse) kao i mikobakterijsku bolest; preostala procjena mora uključivati donorovu anamnezu, uključujući prehrambene navike, moguća izlaganja infektivnim uzročnicima i putovanja.
- Pretransplantacijska obrada primalaca je puno složenija i uključuje obradu na respiratorne viruse i GI patogene.
TRANSPLANTACIJA HEMATOPOETSKIH MATIČNIH STANICA (THMS)
- Patogeneza: Mijeloablativni postupak koji se primjenjuje u okviru THMS ima za posljedicu potpuni nedostatak urođenih i adaptivnih imunih stanica. Ovo prolazno stanje potpune imunološke inkompetencije i postupci koji slijede čine domaćina izrazito osjetljivim prema infekcijama.
- Etiologija: Većina infekcija događa se u unaprijed definiranom vremenskom okviru nakon THMS (Tbl. 79-2).
– Bakterijske infekcije: Infekcijske komplikacije povezane s neutropenijom najčešće su tijekom prvog mjeseca. U nekim se centrima profilaktički primjenjuju antibiotici (npr. fluorirani kinoloni) kako bi se smanjila opasnost od gram-negativne bakterijemije, ali povećava rizik kolitisa uzrokovanog Clostridium difficile.
TABLICA 79-2 UOBIČAJENI IZVORI INFEKCIJA NAKON PRESAĐIVANJA HEMATOPOETSKIH MATIČNIH STANICA
|
|
|
Razdoblje nakon presađivanja
|
|
Mjesto infekcije
|
Rano (<1 mjesec)
|
Srednje (1–4 mjeseca)
|
Kasno (>6 mjeseci)
|
|
Diseminirana
|
Aerobne bakterije (gram-negativne, gram-pozitivne)
|
Candida, Aspergillus, EBV
|
Inkapsulirane bakterije (Streptococcus pneumoniae, Haemophilus influenzae, Neisseria meningitidis)
|
|
Koža i sluznice
|
Herpes simpleks virus
|
Humani herpesvirus tip 6
|
Varicela-zoster virus, HPV (bradavice)
|
|
Pluća
|
Aerobne bakterije (gram-negativne, gram-pozitivne), Candida, Aspergillus, ostale plijesni, HSV
|
CMV, sezonski respiratorni virusi, Pneumocystis, Toxoplasma
|
Pneumocystis, Nocardia, S. pneumoniae
|
|
Gastrointestinalni trakt
|
Clostridium difficile
|
CMV, adenovirus, Bradyrhizobium enterica (stanice pupkovine)
|
EBV, CMV, Bradyrhizobium enterica (stanice pupkovine)
|
|
Bubrezi
|
|
BK virus, adenovirus
|
|
|
Mozak
|
|
HHV-6, Toxoplasma
|
Toxoplasma, JC virus (rijetko)
|
|
Koštana srž
|
|
CMV, HHV-6
|
CMV, HHV-6
|
|
Kratice: HHV-6 = humani herpesvirus tip 6; HPV = humani papiloma virus.
|
- Flora kože i crijeva (npr. S. aureus, koagulaza negativni stafilokoki, E. coli) odgovorna je za većinu infekcija u prvim danima nakon THMS, nakon čega postaju učestaliji nozokomijalni patogeni i filamentozne bakterije (npr. vankomicin-otporni enterokoki, Acinetobacter, otporne gram-negativne bakterije i vrste iz roda Nocardia).
- U kasnom posttransplantacijskom razdoblju (>6 mjeseci nakon rekonstitucije) najčešća je bakterijemija uzrokovana inkapsuliranim bakterijama, posebice među aspleničnim i hipogamaglobulinemičnim bolesnicima.
– Gljivične infekcije: Infekcije gljivama su sve češće nakon prvog tjedna od THMS, posebice među bolesnicima koji dobivaju antibiotike širokog spektra. Najčešće su infekcijama kvascima iz roda Candida, iako i druge otporne gljive (npr. poput Aspergillus, Fusarium) postaju sve češće kad se bolesnicima daje profilaktički flukonazol.
- Produljeno liječenje glukokortikoidima ili drugim imunosupresivnim lijekovima povećava rizik od infekcije s Candida ili Aspergillus, kao i opasnost od reaktivacije endemskih gljiva pa čak i nakon oporavka od neutropenije.
- Za sprječavanje Pneumocystis pneumonije preporučuje se profilaksa trimetoprim-sulfametoksazolom (TMP-SMX; počinje se s 160/800 mg/dan 1 mjesec nakon presađivanja, a u trajanju od barem 1 godine).
– Infekcije parazitima: Profilaksa s TMP-SMX također štiti i od infekcija uzrokovanih s Toxoplasma kao i od nekih kasnih bakterijskih infekcija, uključujući i infekcije s Nocardia, Listeria monocytogenes, S. pneumoniae ili H. influenzae.
- Zbog sve učestalijih internacionalnih putovanja, paraziti koji su tipično ograničeni na određena okolišna područja (npr. uzrokovane sa Strongyloides, Leishmania, Giardia, Cryptosporidium) mogu se nakon THMS reaktivirati.
– Virusne infekcije: Profilaktička primjena aciklovira ili valaciklovira kod HSV-seropozitivnih bolesnika smanjuje učestalost upale sluznica i sprječava pneumoniju i druge infekcije uzrokovane HSV-om.
- Zoster se obično javlja nekoliko mjeseci nakon THMS i dobro odgovara na liječenje aciklovirom.
- HHV-6 može produljiti primanje monocita i trombocita, a može uzrokovati encefalitis ili pneumonitis; učinkovitost antivirusne terapije nije dovoljno istražena.
- CMV infekcija (npr. intersticijska pneumonija, supresija koštane srži, kolitis i odbacivanje presatka) obično se javlja 30-90 dana nakon THMS. Teška je infekcija češća među primaocima alogeničnog presatka i obično je povezana s bolešću presatka protiv primaoca (engl. “graft versus host disease”). Tzv. preemptivna terapija (tj. početak antivirusne terapije tek nakon što se CMV otkrije u krvi) zamijenila je profilaktičku terapiju (liječenje svih transplantiranih kada je ili davatelj ili primaoc seropozitivan) zbog toksičnih učinaka ganaciklovira.
- EBV limfoproliferativna bolest kao i infekcije uzrokovane respiratornim virusima (npr. respiratornim sincicijskim, virusom parainfluenze, metapneumovirusom, influenca virusom ili adenovirusom) također se javljaju. BK virus (polioma virus) može se naći u urinu bolesnika nakon THMS, a povezuje se s hemoragičnim cistitisom.
TRANSPLANTACIJA SOLIDNIH ORGANA
- Patogeneza: Nakon presađivanja solidnih organa, bolesnici ne prolaze kroz stadij neutropenije, kao što se viđa nakon THMS; stoga se infekcije u te dvije skupine bolesnika razlikuju. Međutim, primaoci solidnih organa su imunosuprimirani duže vremensko razdoblje s lijekovima koji kronično oštećuju T-staničnu imunost. Štoviše, trajna HLA nepodudarnost među imunim stanicama primaoca (npr. efektorske T-stanice) i alografta (organa davatelja) čine organ trajno mogućim izvorom infekcije.
- Etiologija: Kao u THMS, rizik za infekciju ovisi o vremenskom intervalu od transplantacije.
– Rane infekcije (<1 mjeseca): Infekcije su uzrokovane ekstracelularnim miroorganizmima, koji potječu iz kirurške rane ili anastomotskih mjesta.
– Infekcije srednjeg razdoblja (1–6 mjeseci): Postaju vidljive posljedice supresije staničnog imuniteta pa su infekcije stečene ili su posljedica reaktivacije - virusa, mikobakterija, endemskih gljiva ili parazita.
- CMV uzrokuje tešku sistemsku bolest ili infekciju presađenih organa, što pojačava odbacivanje organa, dovodeći do potrebe za pojačanom imunosupresijom, koja, s druge strane, pojačava umnažanje CMV-a.
- Dijagnoza, liječenje i profilaksa infekcije s CMV-om su ključni za prekidanje ovog kruga.
– Kasne infekcije (>6 mjeseci): Infekcije u ovom razdoblju su slične onima u bolesnika s kroničnim poremećajem T-stanične imunosti (npr. Listeria, Nocardia, Rhodococcus, mikobakterije, različite gljive i ostali unutarstanični mikroorganizmi).
- EBV limfoproliferativna bolest događa se najčešće u bolesnika koji su primili transplantat srca ili pluća (kao i najintenzivniji imunosupresivni režim); u ovim slučajevima, imunosupresiju bi trebalo smanjiti ili ukinuti, ako je to moguće i razmišljati o mogućem liječenju s anti-B protutijelima.
- Profilaksa za pneumoniju uzrokovanu Pneumocystis od najmanje godinu dana se općenito preporuča za sve primaoce solidnih organa.
- Incidencija tuberkuloze unutar prvih 12 mjeseci nakon transplantacije solidnog organa je veća nego nakon THMS, a odražava prevaenciju tuberkuloze u lokalnoj populaciji.
- Specifična razmatranja: Iako gore navedene informacije vrijede za primaoce bilo kojeg organa, postoje neka razmatranja specifična za pojedine organe.
– Presađivanje bubrega: TMP-SMX profilaksa tijekom prvih 4-6 mjeseci smanjuje incidenciju infekcija ranog i srednjeg razdoblja, posebice infekcije mokraćnog sustava (IMS) koje su u svezi s anatomskim promjenama nakon kirurškog zahvata. CMV je predominantan patogen srednjeg razdoblja; infekcija se javlja u 50% bolesnika koji su primili bubreg, a koji 1-4 mjeseca nakon transplantacije postaju febrilni, zbog čega mnogi centri koriste valganciklovir u profilaksi visokorizičnih bolesnika. BK virurija i viremija, koje se najčešće dijagnosticiraju u kasnoj fazi, povezane su sa strikturama uretera, nefropatijom, vaskulopatijom i zahtijevaju smanjenje imunosupresije kako bi se smanjila učestalost odbacivanja.
– Transplantacija srca: Medijastinitis, najčešće uzrokovan florom kože te rijetko s Mycoplasma hominis, je rana komplikacija transplantacije srca. Ukupna incidencija toksoplazmoze (infekcija srednjeg razdoblja) je jako visoka kada se radi o transplantaciji srca pa se serološki probir i profilaksa (npr. TMP-SXT) preporučuju.
– Transplantacija pluća: Bolesnici kojima su transplantirana pluća predisponirani su pneumoniji i medijastinitisu u ranom razdoblju. Visoka incidencija CMV bolesti (75-100% ako su donor ili primaoc seropozitivni) ukazuje na važnost antivirusne profilakse; kasna bolest može se dogoditi nakon što se s profilaksom prekine, iako je bolesnici lakše podnose jer je imunosupresija slabija.
– Transplantacija jetre: bakterijski apscesi i peritonitis su česte komplikacije i najčešće su rezultat istjecanja žuči. Bolesnici kojima je transplantirana jetra četo dobiju gljivične imfekcije što korelira s uzimanjem glukokortikoida preoperativno, dugotrajnom antibiotskom terapijom i visokom imunosupresijom. Rekurentni (reaktivirani) hepatitis B ili C su problem; iako davanje hepatitis B imunoglobulina i profilaksa s antiviroticima može spriječiti reinfekciju hepatitis B virusom, reinfekcija s hepatitis C virusom događa se u svih bolesnika.
IMUNIZACIJA U IMUNOSUPRIMIRANIH BOLESNIKA
Preporuke za cijepljenje bolesnika koji boluju od karcinoma i primaju kemoterapiju, bolesnika koji imaju Hodgkinovu bolest te u bolesnika kojima je urađena THMS, navedena je u Tbl. 79-3. U primalaca presatka solidnog organa trebalo bi prije imunosupresije primijeniti uobičajena cjepiva i docjepljivanja. Bolesnicima na trajnoj imunosupresiji treba ponoviti cijepljenje protiv pneumokoka svakih 5 godina i ne smiju dobiti živo cjepivo.
TABLICA 79-3 CIJEPLJENJE ONKOLOŠKIH I TRANSPLANTIRANIH BOLESNIKA KOJI PRIMAJU KEMOTERAPIJUa
|
|
|
Indikacije
|
|
Cjepivo
|
Intenzivna kemoterapija
|
Hodgkinova bolest
|
Transplantacija hematopoetskih matičnih stanica
|
|
Difterija-tetanusb
|
Primarni niz i docjepljivanje po potrebi
|
Nema posebnih preporuka
|
Tri doze 6-12 mjeseci nakon presađivanja
|
|
Poliomijelitisc
|
Potpuni primarni niz i docjepljivanje
|
Nema posebnih preporuka
|
Tri doze 6-12 mjeseci nakon presađivanja
|
|
Haemophilus influenzae tip b konjugirano
|
Primarni niz i docjepljivanje za djecu
|
Jedna doza za odrasle
|
Tri doze 6-12 mjeseci nakon presađivanja (u razmaku od 1 mj.)
|
|
HPV
|
Kvadrivalentno HPV cjepivo odobreno je muškarcima i ženama od 9-26 godina. Provjerite CDC web stranicu (www.cdc.gov/vaccines) za osvježene informacije
|
Kvadrivalentno HPV cjepivo odobreno je muškarcima i ženama od 9-26 godina. Provjerite CDC web stranicu (www.cdc.gov/vaccines) za osvježene informacije
|
Kvadrivalentno HPV cjepivo odobreno je muškarcima i ženama od 9-26 godina. Provjerite CDC web stranicu (www.cdc.gov/vaccines) za osvježene informacije
|
|
Hepatitis A
|
Kao što je indicirano za normalnog domaćina na temelju zanimanja i životnih navika
|
Kao što je indicirano za normalnog domaćina na temelju zanimanja i životnih navika
|
Kao što je indicirano za normalnog domaćina na temelju zanimanja i životnih navika
|
|
Hepatitis B
|
Jednako kao za normalnog domaćina
|
Kao što je indicirano za normalnog domaćina na temelju zanimanja i životnih navika
|
Tri doze daju se 6-12 mjeseci nakon transplantacije
|
|
PCV13
PPSV23d
|
Dovršiti seriju ako je moguće prije kemoterapije
|
Splenektomirani moraju dobiti PPSV23.
|
Tri doze PCV13, počinje se 3-6 mjeseci nakon transplantacije, a potom doza PPSV23 najmanje 8 tjedana kasnije. Druga doza PPSV23 može se dati 5 godina kasnije.
|
|
4-valentno meningokoknoe
|
Trebalo bi se dati splenektomiranim bolesnicima i bolesnicima koji žive u endemskim područjima, uklju-čujući studente iz studentskih domova
|
Trebalo bi se dati splenektomiranim bolesnicima i bolesnicima koji žive u endemskim područji-ma, uključujući studente iz studentskih domova. Dodatna doza može se dati 5 godina kasnije.
|
Trebalo bi se dati splenektomiranim bolesnicima i bolesnicima koji žive u endemskim područjima, uključujući studente iz studentskih domova. Dodatna doza može se dati 5 godina kasnije.
|
|
Gripa
|
Sezonska imunizacija
|
Sezonska imunizacija
|
Sezonska imunizacija (Sezonska doza se preporuča najranije poslije 4 mjeseca od transplantacije; ako se da <6 mjeseci od transplantacije preporuča se dodatna doza.)
|
|
Morbili/parotitis/rubela
|
Kontraindicirano
|
Kontraindicirano tijekom kemoterapije
|
Nakon 24 mjeseca u bolesnika bez bolesti presatka protiv primaoca
|
|
Varicela-zoster virusf
|
Kontraindiciranog
|
Kontraindicirano
|
Kontraindicirano (CDC preporučuje korištenje ovisno o pojedinom slučaju uz reevaluaciju)
|
|
aPosljednje preporuke Odbora za savjete o imunizaciji i CDC smjernice mogu se naći na http://www.cdc.gov/vaccines.
bJedna doza tetanus-difterija-acelularni pertusis (TDaP), nakon koje se daje tetanus-difterija (Td) svakih 10 godina, preporuča se odraslim bolesnicima.
cŽiva cjepiva su kontraindicirana; moraju se koristiti inaktivirana cjepiva.
dDva tipa cjepiva se koriste u sprječavanju pneumokokne bolesti. Konjugirano cjepivo aktivno prema 13 serotipova (13-valentno pneumokokno konjugirano ili PCV13) trenutno se u tri odvojene doze daje djeci. Polisaharidno cjepivo aktivno protiv 23 serotipa (23-valentna polisaharidno pneumokokno cjepivo ili PPSV23) potiče razinu protutijela nižu od one koju postiže konjugirano cjepivo, a imunost kraće traje. Budući da ablativna kemoterapija koja se daje primaocima hematopetskih matičnih stanica eradicira imunološku memoriju, takvim se bolesnicima preporuča revakcinacija. Cijepljenje je puno učinkovitije nakon imunološke rekonstitucije; ipak, zbog potrebe prevencije ozbiljne bolesti, pneumokokno cjepivo se daje 6-12 mjeseci nakon transplantacije u većini slučajeva. Budući da PPSV23 uključuje serotipove koji nisu prisutni u PCV13, primaoci koštane srži moraju dobiti PPSV23 najmanje 8 tjedana nakon zadnje doze PCV13. Iako titar protutijela nakon PPSV23 brzo opada, iskustva s multiplim dozama PPSV23 su ograničena, kao što su i podatci o sigurnosti, toksičnosti ili učinkovitosti ovakvog liječenja. Zbog toga, CDC trenutno preporuča davanje još jedne doze PPSV23 najmanje 5 godina od zadnje doze imunokompromitiranima što uključuje i transplantirane, bolesnike s Hodgkinovom bolešću, multiplim mijelomom, limfomom ili općenito malignomom. Osim te dodatne doze, u ovom trenutku ne preporučuje se više doza.
eMeningokokno konjugirano cjepivo. MenACWY se preporuča odraslima ≤55 godina dok se meningokokno polisahardidno cjepivo (MPSV4) preporuča onima od 56 i više godina.
f Uključuje i varicella cjepivo za djecu i zoster cjepivo za odrasle.
gKontaktirati proizvođača za više informacija o korištenju u djece s akutnom limfocitnom leukemijom.
Kratice: CDC = Centar za kontrolu i prevenciju bolesti; HPV = humani papiloma virus; PCV = pneumokokno konjugirano cjepivo; PPSV = pneumokokno polisaharidno cjepivo.
|
Opširnije vidi u Finberg RW: Infekcije u bolesnika s karcinomom, Pogl. 104, str. 484; i Finberg RW, Fingeroth J: Infekcije u transplantiranih, Pogl. 169, str. 919, u HPIM-19..